Десятки биотехнологических компаний и научных институтов наперегонки с пандемией создают разные варианты вакцин от нового коронавируса SARS‑CoV‑2. Разбираемся, какие технологии используют для их разработки, сколько времени пройдёт до момента, когда от COVID‑19 можно будет делать прививки, и сможет ли будущая вакцина остановить пандемию.
Каждый раз, когда человечество сталкивается с новой инфекцией, одновременно стартуют три гонки: за лекарством, тест‑системой и вакциной. На предыдущей неделе в России начались Научный центр Роспотребнадзора начал испытания вакцины против нового коронавируса испытания антикоронавирусной вакцины на животных, а в США — уже на людях NIH clinical trial of investigational vaccine for COVID‑19 begins . Значит ли это, что победа над эпидемией близка?
По данным ВОЗ, около 40 лабораторий в мире заявили DRAFT landscape of COVID‑19 candidate vaccines – 20 March 2020 о том, что ведут разработку вакцин против коронавируса. И несмотря на то, что среди них есть явные лидеры — например, китайская компания CanSino Biologics, которая получила RECOMBINANT NOVEL CORONAVIRUS VACCINE (ADENOVIRUS TYPE 5 VECTOR) APPROVED FOR CLINICAL TRIAL разрешение на испытания на людях, и американская Moderna, которая их уже начала, — сейчас сложно предсказать, какая из компаний победит в этой гонке, а главное — обгонит ли разработка вакцин распространение коронавируса. Успех в этом забеге зависит не в последнюю очередь от выбора оружия, то есть от принципа, на котором построена вакцина.
Мёртвый вирус — плохой вирус
В школьных учебниках обычно пишут, что для прививок используют убитый или ослабленный возбудитель инфекции. Но эта информация несколько устарела. «Инактивированные („убитые“. — Прим. N+1.) и аттенюированные (ослабленные. — Прим. N+1.) вакцины были придуманы и введены в середине прошлого века, и их трудно считать современными, — объясняет в разговоре с N+1 Ольга Карпова, заведующая кафедрой вирусологии биологического факультета МГУ имени Ломоносова. — Это дорого. Это сложно в транспортировке и хранении, многие вакцины доезжают до мест, где они нужны (если мы говорим, например, об Африке) в таком состоянии, когда они никого уже не защищают».
Кроме того, это небезопасно. Для того, чтобы получить высокую дозу «убитого» вируса, необходимо сначала обзавестись большими количествами живого, а это повышает требования к оснащению лаборатории. Потом его нужно обезвредить — для этого используют, например, ультрафиолет или формалин.
Но где гарантия, что среди множества «мёртвых» вирусных частиц не останется сколько‑то способных вызвать болезнь?
С ослабленным возбудителем всё ещё сложнее. Сейчас для того, чтобы ослабить, вирус заставляют мутировать, а потом отбирают наименее агрессивные штаммы. Но при этом получается вирус с новыми свойствами, и не все их можно предсказать заранее. Опять же, где гарантия, что, оказавшись внутри организма, вирус не продолжит мутировать и не произведёт «потомство», ещё более «злое», чем оригинал?
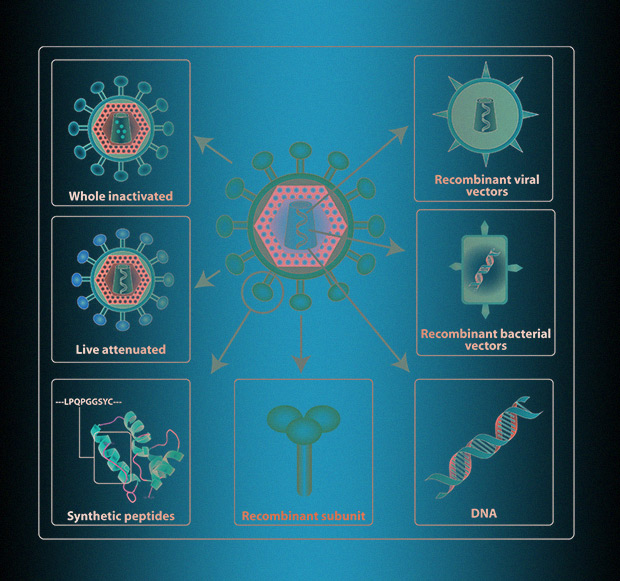
Поэтому как «убитые», так и «недобитые» вирусы сегодня используют редко. Например, среди современных вакцин от гриппа «ослабленные возбудители» находятся Next‑generation influenza vaccines: opportunities and challenges в меньшинстве — так устроены лишь 2 из 18 вакцин, одобренных в Европе и США к 2020 году. Из более 40 проектов вакцин от коронавируса по такому принципу устроена лишь одна — ей занимается индийский Институт сывороток.
Разделяй и вакцинируй
Гораздо безопаснее познакомить иммунную систему не с целым вирусом, а с отдельной его частью. Для этого нужно подобрать белок, по которому «внутренняя полиция» человека сможет безошибочно распознать вирус. Как правило, это поверхностный белок, с помощью которого патоген проникает внутрь клеток. Затем нужно заставить какую‑нибудь культуру клеток произвести этот белок в промышленных масштабах. Это делают с помощью генной инженерии, поэтому такие белки называют генноинженерными, или рекомбинатными.
«Я считаю, что вакцины должны быть обязательно рекомбинантными, и никак иначе, — говорит Карпова. — Притом это должны быть вакцины на носителях, то есть белки вируса должны находиться на каком‑то носителе. Дело в том, что сами по себе они (белки) не иммуногенные. Если в качестве вакцины использовать низкомолекулярные белки, на них не будет вырабатываться иммунитет, организм не будет на них реагировать, поэтому частицы‑носители абсолютно необходимы».
В качестве такого носителя исследователи из МГУ предлагают использовать вирус табачной мозаики Вирус табачной мозаики — «Википедия» (это, кстати, самый первый открытый людьми вирус). Обычно он похож на тонкую палочку, но при нагревании принимает форму шарика. «Он стабилен, у него уникальные адсорбционные свойства, он притягивает к себе белки, — рассказывает Карпова. — На его поверхности можно разместить небольшие белки, те самые антигены». Если покрыть вирус табачной мозаики белками коронавируса, то для организма он превращается в имитацию вирусной частицы SARS‑CoV‑2. «Вирус табачной мозаики, — отмечает Карпова, — является для организма эффективным иммуностимулятором. В то же время, поскольку вирусы растений не могут заражать животных, в том числе человека, мы делаем абсолютно безопасный продукт».

Безопасность разных методов, связанных с рекомбинантными белками, сделала их самыми популярными — не менее десятка компаний сегодня пытаются получить такой белок для коронавируса. Кроме того, многие используют другие вирусы‑носители — например, аденовирусные векторы или даже модифицированные «живые» вирусы кори и оспы, которые заражают клетки человека и размножаются там вместе с белками коронавируса. Тем не менее эти методы не самые быстрые, потому что необходимо наладить поточное производство белков и вирусов в клеточных культурах.
Голые гены
Этап производства белка в культуре клеток можно сократить и ускорить процесс, если заставить клетки организма производить вирусные белки самостоятельно. По такому принципу работают генотерапевтические вакцины — в клетки человека можно встроить «голый» генетический материал — вирусную ДНК или РНК. ДНК обычно вводят в клетки с помощью электропорации, то есть вместе с уколом человек получает лёгкий разряд, в результате проницаемость клеточных мембран увеличивается, и нити ДНК попадают внутрь. РНК доставляют с помощью липидных пузырьков. Так или иначе, клетки начинают производить вирусный белок и демонстрировать его иммунной системе, а она разворачивает иммунный ответ даже в отсутствие вируса.
Этот метод довольно новый, в мире ещё нет вакцин, которые работали бы по такому принципу.
Тем не менее сразу семь компаний, по данным ВОЗ, пробуют сделать вакцину от коронавируса на его основе. По этому пути идёт Moderna Therapeutics — американский лидер гонки за вакциной. Его же выбрали для себя ещё три участника гонки из России: научный центр «Вектор» в Новосибирске (по данным Роспотребнадзора, он проверяет целых шесть дизайнов вакцин одновременно, и один из них — на основе РНК), компания Biocad и Научно‑клинический центр прецизионной и регенеративной медицины в Казани.
«Создать вакцину в принципе не так сложно, — считает директор Центра, профессор кафедры генетики Института фундаментальной медицины и биологии КФУ Альберт Ризванов. — Генно‑терапевтические вакцины по скорости разработки самые быстрые, потому что достаточно создать генетическую конструкцию». Вакцина, над которой работают в Центре, должна выстрелить по нескольким мишеням разом: в клетки вводят нить ДНК с несколькими вирусными генами одновременно. В результате клетки будут производить не один вирусный белок, а сразу несколько.
Кроме того, по словам Ризванова, ДНК‑вакцины могут оказаться дешевле прочих в производстве. «Мы, по сути своей, как Space X, — шутит учёный. — У нас разработка прототипа стоит всего несколько миллионов рублей. Правда, создание прототипа — это только верхушка айсберга, а тестирование с живым вирусом — это совсем другой порядок».
Превратности и хитрости
Как только вакцины из теоретических разработок превращаются в объект исследований, препятствия и ограничения начинают расти, как грибы. И финансирование — только одна из проблем. По словам Карповой, в МГУ уже есть образец вакцины, но для дальнейших испытаний понадобится сотрудничество с другими организациями. На следующем этапе они планируют проверять безопасность и иммуногенность, и это можно сделать в стенах университета. Но как только потребуется оценить эффективность вакцины, то придётся работать с патогеном, а это в учебном заведении запрещено.
Кроме того, потребуются специальные животные. Дело в том, что обычные лабораторные мыши болеют далеко не всеми человеческими вирусами, и картина болезни тоже может сильно отличаться. Поэтому вакцины часто тестируют на хорьках. Если же ставить целью работу именно с мышами, то необходимы генетически‑модифицированные мыши, которые несут на своих клетках точь‑в‑точь те рецепторы, за которые «цепляется» коронавирус в организме пациента. Эти мыши стоят недёшево Ace2 CONSTITUTIVE KNOCKOUT (десяток или два десятка тысяч долларов за линию). Правда, иногда можно сэкономить — закупить всего несколько особей и размножить их в лаборатории — но это удлиняет этап доклинических испытаний.

И если решить проблему финансирования ещё в наших силах, то время пока остаётся непреодолимой трудностью. По словам Ризванова, на разработку вакцин обычно уходят месяцы и годы. «Редко меньше года, обычно больше», — уточняет он. Руководитель Федерального медико‑биологического агентства (там разрабатывают вакцину на основе рекомбинантного белка) Вероника Скворцова предположила ФМБА России получит первые результаты испытаний прототипов вакцины против коронавируса в июне 2020 года , что готовая вакцина может появиться через 11 месяцев.
Есть несколько этапов, на которых процесс можно ускорить. Самый очевидный — разработка. Американская компания Moderna вырвалась вперёд, потому что давно занимается созданием мРНК‑вакцин. И чтобы сделать ещё одну, им оказалось достаточно расшифрованного генома нового вируса. Российские коллективы из Москвы и Казани тоже не первый год работают над своей технологией и опираются на результаты испытаний своих предыдущих вакцин от других болезней.
Идеальным вариантом была бы платформа, которая позволяет быстро создавать новую вакцину по шаблону. Подобные планы вынашивают, в том числе, исследователи из МГУ.
«На поверхности своей частицы, — рассказывает Карпова, — мы можем можем разместить белки нескольких вирусов и защищать одновременно от COVID‑19, SARS и MERS. Мы даже думаем о том, что можно предотвратить такие вспышки в дальнейшем. Существует 39 коронавирусов, часть из них близка к коронавирусам человека, и совершенно понятно, что такое преодоление видового барьера („перепрыгивание“ вируса от летучих мышей к человеку. — Прим. N+1.). Но если будет такая вакцина, как конструктор Lego, мы можем поместить на неё белок какого‑то вируса, который где‑то возник. Мы это сделаем в течение двух месяцев — заменим или добавим эти белки. Если бы такая вакцина была в декабре 2019 года, и прошли бы вакцинации людей хотя бы в Китае, дальше это бы не распространилось».
Следующий этап — доклинические испытания, то есть работа с лабораторными животными. Это не самый долгий процесс, но за его счёт можно выиграть, если совместить с клиническими испытаниями на людях. Именно это сделала Moderna — компания ограничилась быстрой проверкой на безопасность и сразу перешла к исследованиям на людях. Однако стоит помнить, что препарат, который она пробует, относится к самым безопасным. Поскольку Moderna не использует ни вирусы, ни рекомбинантные белки, то очень невелик шанс, что у добровольцев возникнут побочные эффекты — иммунной системе просто не на что агрессивно реагировать. Худшее, что может произойти, — вакцина окажется неэффективной. Но это ещё предстоит проверить.
А вот производство вакцин, судя по всему, ограничивающим этапом не является. «Это не сложнее, чем обычное биотехнологическое производство рекомбинантных белков», — объясняет Ризванов. Произвести миллион доз такой вакцины, по его словам, завод может за единицы месяцев. Ольга Карпова даёт похожую оценку: три месяца для миллиона доз.
А нужна ли вакцина?
Стоит ли сокращать клинические испытания — вопрос спорный. Во‑первых, это сам по себе процесс небыстрый. Во многих случаях вакцину нужно вводить в несколько этапов: если вирус не размножается сам по себе внутри организма, то он быстро выводится, и его концентрация оказывается недостаточной Avian Influenza A Virus Pandemic Preparedness and Vaccine Development , чтобы вызвать серьёзный иммунный ответ. Поэтому даже простая проверка эффективности займёт не меньше нескольких месяцев, а за безопасностью вакцины для здоровья добровольцев врачи собираются следить целый год.
Во‑вторых, COVID‑19 — тот самый случай, когда ускорять испытания на людях многим кажется нецелесообразным.
Смертность от болезни сегодня оценивают в единицы процентов, и это значение, вероятно, ещё будет снижено, как только станет ясно, какое количество людей перенесло болезнь бессимптомно. Но вакцину, если она будет изобретена сейчас, придётся ввести миллионам людей, и даже небольшие побочные эффекты могут вылиться в количество болезней и смертей, сопоставимое с самой инфекцией. А новый коронавирус далеко не настолько «зол», чтобы, по выражению Ризванова, «совсем уж откидывать в сторону все соображения безопасности». Учёный полагает, что в сложившейся сегодня ситуации наиболее эффективен карантин.
Впрочем, по словам Карповой, в ближайшее время в вакцине нет острой необходимости. «Вакцинировать людей во время пандемии не нужно, это не соответствует эпидемическим правилам», — объясняет она.
С ней согласна Галина Кожевникова, заведующая кафедрой инфекционных болезней РУДН. «В период эпидемии не рекомендуется вообще никакая вакцинация, даже плановая, которая входит в календарь прививок. Потому что нет никакой гарантии, что человек не находится в инкубационном периоде, а если в этот момент применить вакцину, возможны нежелательные явления и сниженная эффективность прививки», — сказала Кожевникова, отвечая на вопрос N+1.
Бывают случаи, добавила она, когда необходима экстренная вакцинация по жизненным показаниям, в ситуации, когда речь идёт о жизни и смерти. Например, во время вспышки сибирской язвы в Свердловске в 1979 году вакцинировали всех подряд, тысячи людей экстренно прививали и в 1959 году в Москве во время вспышки натуральной оспы, привезённой Кокорекин, Алексей Алексеевич — «Википедия» из Индии художником Алексеем Кокорекиным.
«Но коронавирус — это абсолютно не такая история. По тому, что происходит, мы видим, что эта эпидемия развивается по классическим законам острого респираторного заболевания», — говорит Кожевникова.
Таким образом, разработчики вакцин всегда находятся в неудобной ситуации. Пока вируса нет, вакцину создать практически невозможно. Как только вирус появился, оказывается, что это необходимо было сделать позавчера. А когда он отступает, то производители теряют своих клиентов.
Тем не менее вакцину необходимо сделать. Этого не произошло во время предыдущих вспышек коронавирусных инфекций — и MERS, и SARS слишком быстро закончились, и исследования лишились финансирования. Но если случаев SARS в мире не наблюдалось с 2004 года, то последний случай MERS датируют 2019 годом, и никто не может гарантировать, что вспышка не повторится. Кроме того, вакцина от предыдущих инфекций может стать стратегической платформой для разработки будущих вакцин.
Карпова отмечает, что даже после затухания этой вспышки COVID‑19 возможна ещё одна. И вот в таком случае государство должно иметь наготове вакцину. «Это не та вакцина, которой все люди будут прививаться, как от гриппа, — уточняет она. — Но в экстренной ситуации при новой вспышке такая вакцина у государства должна быть, так же как и тест‑система».